¿Realmente tienes calor?
Valoración de la comunidad:
Última Actualización:
6 de Febrero de 2025 a las 16:55¿Realmente tienes calor?
Aprendizaje esperado: analiza el calor como energía.
Énfasis: identificar las diferencias entre los conceptos de temperatura y calor.
¿Qué vamos a aprender?
Reconocerás la diferencia entre el calor y la temperatura. Además, analizarás su concepto y sus características.
¿Qué hacemos?
Para diferenciar y usar correctamente las palabras “temperatura” y “calor”, primero debes entender los orígenes de estos conceptos. Para ello, deberás dar un vistazo a nuestro pasado y conocer cuál fue la fuente de calor más próxima al hombre.
Mucho antes de cualquier invento o descubrimiento científico, el hombre tenía la necesidad de adaptarse al ecosistema del cual formaba parte, sin embargo, las condiciones de vida eran extremas, así como los peligros a los que se enfrentaban.
En la actualidad, se sabe que el Homo Erectus descubrió el fuego hace 1.6 millones de años. Y con este descubrimiento se abrió un futuro completamente nuevo, fue uno de los descubrimientos más importantes.
El concepto de “calor” comenzó a estudiarse por el químico francés Antoine Lauren de Lavoisier en 1789, en su libro titulado “Tratado elemental de la química”. En esta obra, mencionó que el calor era producto de un fluido elástico al que llamo calórico.

En 1798, Benjamín Thompson propuso que el calor no era una sustancia elástica sino un producto del movimiento.

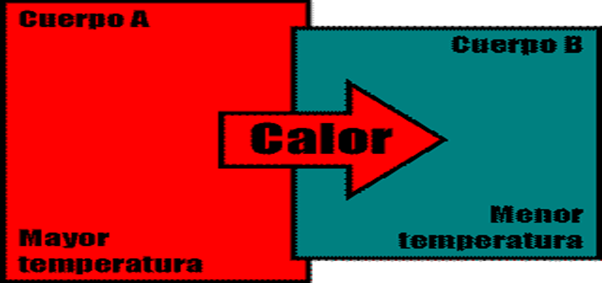
Actualmente, la teoría del calórico ha sido abandonada y se sabe que el calor es la energía que se transmite entre dos o más cuerpos y va del que tiene mayor temperatura al que tiene menor temperatura.
El calor es una forma de energía necesaria para que ocurran algunos procesos naturales, como la formación de rocas o la existencia de las corrientes marinas. Además, permite realizar diversas actividades y es útil para el funcionamiento de algunas máquinas, que a su vez liberan energía térmica; por ejemplo, las que ayudan a que determinados transportes recorran grandes distancias en tiempos cortos
Para reforzar este concepto, observa el siguiente video.
- ¿Es lo mismo calor que temperatura?
https://youtu.be/haWkRRSBrCk
El calor es una transmisión de energía, lo cual es muy diferente a la temperatura. La energía calorífica o térmica incrementa la temperatura de los objetos y puede provocar cambios en ellos.
Ahora que sabes qué es el calor, puedes emplear correctamente esta palabra, pero ¿cuándo es correcto ocupar a la temperatura?
El concepto de temperatura es un poco más complejo, pero no imposible de entender. La medición de la temperatura tuvo sus inicios con uno de los personajes más importantes en la física llamado Galileo Galilei.
Galileo construyó en 1592 un instrumento llamado termoscopio, este experimento fue el primer termómetro creado, pero no era tan preciso pues decía relativamente las condiciones del ambiente.
Galileo descubrió que la densidad de un líquido cambia según la temperatura, rápidamente se dio cuenta de que podría aprovechar este fenómeno para crear un instrumento destinado a medir la temperatura ambiente. Así fue como nació el denominado “termoscopio de Galileo”.
El termoscopio consistía en una esfera de vidrio con aire, soldada a un tubo delgado que se sumergía por el extremo abierto de un recipiente con agua. Si se calentaba la esfera de vidrio, por ejemplo, entre las manos, el aire en su interior se dilataba y el agua en el tubo bajaba su nivel y a medida que iba disminuyendo la temperatura de la esfera, el aire se comprimía hacia su valor inicial, y el agua ascendía en el tubo sobre el nivel que tenía el recipiente con agua.
El termoscopio fabricado por Galileo carecía de una medida que reflejara matemáticamente a qué temperatura se encontraban los cuerpos. Pero dio las bases para que futuros científicos estudiaran este campo.
Por ejemplo, Daniel Gabriel Fahrenheit quien invento el primer termómetro moderno en 1709 y en 1714 creo el primer termómetro de mercurio, pero diez años después introdujo la escala de temperatura que lleva en honor su nombre, esta escala establece que las temperaturas de congelación y ebullición del agua son de 32° F y 212° F, respectivamente.
Además de esta escala, también se cuenta con la escala Celsius propuesta por Anders Celsius, la cual considera que el punto de ebullición del agua es de 100°C y el punto de congelación es de 0°C.
Por último, pero no menos importante, se tiene la escala de Kelvin, cuyo nombre es dado en honor a William Thomson, conocido como lord Kelvin por sus aportaciones a la ciencia. La escala de Kelvin comienza en el cero absoluto (0 K), temperatura que equivale -273.15° en la escala de Celsius, y a -459.67° en la de Fahrenheit.
Mientras las escalas de Celsius y Fahrenheit son de uso cotidiano, la de Kelvin se emplea preferentemente en el ámbito científico.
Para ilustrar lo anterior, observa la siguiente capsula.
Termómetro.
https://youtu.be/cPqr6ciL9m0
La temperatura, es la medida del nivel de energía cinética de las moléculas de un cuerpo, cuanto más rápido se muevan las moléculas que integran al cuerpo, mayor será su temperatura y si se desea aumentar la temperatura de un cuerpo se debe aplicar calor.
Las moléculas de agua en una taza de café caliente tienen una mayor energía cinética promedio que las moléculas de agua en un vaso con agua helada, lo que también significa que están moviéndose a una velocidad más alta. La temperatura también es una propiedad intensiva. Esto significa que no depende de qué tanta cantidad tengas de una sustancia.
Por esta razón, se puede utilizar el punto de fusión para poder identificar una sustancia pura: la temperatura a la cual se derrite es una propiedad de la sustancia que no depende de la masa de una muestra.
A nivel atómico, las moléculas en cada objeto están constantemente en movimiento y chocando entre sí. Cada vez que chocan, pueden transferir energía cinética. Cuando dos sistemas están en contacto, se va a transferir calor del sistema más caliente al más frío por medio de choques moleculares.
La energía térmica va a fluir en esa dirección hasta que los dos objetos están a la misma temperatura. Cuando esto ocurre, se dice que están en equilibrio térmico.
En el lenguaje común, se utiliza calor para referirse a la temperatura y temperatura para decir que hubo transferencia de calor.
A continuación, observa el siguiente video para recapitular en las diferencias que hay entre la temperatura y el calor. - Calor como forma de energía.
Recapitulando, el calor es la energía total del movimiento molecular en una sustancia, mientras temperatura es una medida de la energía molecular media. El calor depende de la velocidad de las partículas, su número, su tamaño y su tipo. La temperatura no depende del tamaño, del número o del tipo.
Por ejemplo, la temperatura de un vaso pequeño de agua puede ser la misma que la temperatura de un tinaco lleno agua, pero el agua del tinaco tiene más calor porque tiene más agua y por lo tanto más energía térmica total.
Además, el calor es lo que hace que la temperatura aumente o disminuya. Si se añade calor, la temperatura aumenta. Si se quita calor, la temperatura disminuye.
Ahora que reconoces la diferencia entre el calor y temperatura, comparte con tu familia que significan ambos términos.
El reto de hoy:
Realiza una tabla comparativa en la que coloques las principales diferencias entre calor y temperatura.
Analiza y responde la siguiente cuestión:
¿Qué objeto tiene más calor, un trozo de hielo de 10 kilos o una taza de agua hirviendo?
¡Buen trabajo!
Gracias por tu esfuerzo.
Para saber más:
Lecturas


Login to join the discussion